1.ÎäÎx∆Ω∫‚≈cÀÆΩ‚∆Ω∫‚µƒ±»ð^“é(gu®©)¬…
|
|
ÎäÎx∆Ω∫‚
|
ÀÆΩ‚∆Ω∫‚
|
|
åç(sh®™)¿˝
|
H2SÀƻГ∫(0.1 mol·L£≠1)
|
Na2SÀƻГ∫(0.1 mol·L£≠1)
|
|
—–æøå¶(du®¨)œÛ
|
»ıÎäΩ‚Ÿ|(zh®¨)(»ıÀ·�����°¢»ıâA�����°¢ÀÆ)
|
èä(qi®¢ng)ÎäΩ‚Ÿ|(zh®¨)(»ıÀ·˚}���°¢»ıâA˚})
|
|
åç(sh®™)Ÿ|(zh®¨)
|
»ıÀ·  H£´£´»ıÀ·∏˘Îx◊” H£´£´»ıÀ·∏˘Îx◊”
»ıâA OH£≠£´Íñ(y®¢ng)Îx◊” OH£≠£´Íñ(y®¢ng)Îx◊”
Îx◊”ªØÀŸ¬ =∑÷◊”ªØÀŸ¬
|
.jpg)
|
|
≥Ã∂»
|
À·(âA)‘Ω»ı����£¨ÎäÎx≥Ã∂»‘Ω–°∂ý‘™»ıÀ·
“ªºâ(j®™)ÎäÎx£æ∂˛ºâ(j®™)ÎäÎx
|
å¶(du®¨)ë™(y®©ng)À·(âA)‘Ω»ı��£¨ÀÆΩ‚≥Ã∂»‘Ω¥Û∂ý‘™»ıÀ·∏˘
“ªºâ(j®™)ÀÆΩ‚£æ∂˛ºâ(j®™)ÀÆΩ‚
|
|
ƒÐ¡ø◊ɪØ
|
Œ¸ü·
|
Œ¸ü·
|
|
±Ì þ_(d®¢) Ω
|
ÎäÎx∑Ω≥Ã Ω£∫¢Ÿ
¢⁄∂ý‘™»ıÀ·∑÷≤ΩÎäÎx
H2S H£´£´HS£≠ H£´£´HS£≠
HS£≠ H£´£´S2£≠ H£´£´S2£≠
|
ÀÆΩ‚Îx◊”∑Ω≥Ã Ω£∫¢Ÿ
¢⁄∂ý‘™»ıÀ·∏˘∑÷≤ΩÀÆΩ‚
¢€Æa(ch®£n)ŒÔ“ª∞„≤ªòÀ(bi®°o)“↑”ªÚ“↓”
S2£≠£´H2O HS£≠£´OH£≠ HS£≠£´OH£≠
HS£≠£´H2O H2S£´OH£≠ H2S£´OH£≠
|
|
¡£◊”ù‚∂»
|
¥Û–°
±»ð^
|
c(H2S)£æc(H£´)£æc(HS£≠)£æc(S2£≠)£æc(OH£≠)
|
c(Na£´)£æc(S2£≠)£æc(OH£≠)£æc(HS£≠)£æc(H2S)
|
|
Îä∫… ÿ∫„ Ω
|
c(H£´)=c(HS£≠)£´2c(S2£≠)£´C(OH£≠)
|
c(Na£´)£´c(H£´)=c(HS£≠)£´2c(S2£≠)£´c(OH£≠)
|
|
ŒÔ¡œ ÿ∫„ Ω
|
c(H2S)£´c(HS£≠)£´c(S2£≠)=0. mol£≠1
|
c(S2£≠)£´c(HS£≠)£´c(H2S)=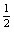 c(Na£´)=0.1 mol·L£≠1 c(Na£´)=0.1 mol·L£≠1
|
|
“H” ÿ∫„ Ω
|
c(H£´)=c(HS£≠)£´2c(S2£≠)£´c(OH£≠)
|
c(H£´)£´c(HS£≠)£´2c(H2S)=c(OH£≠)
|
|
”∞Ìë“ÚÀÿ
|
úÿ∂»
|
…˝úÿ�£¨¥ŸþM(j®¨n)ÎäÎx����£¨Îx◊”ù‚∂»‘ˆ¥Û
|
…˝úÿ£¨¥ŸþM(j®¨n)ÀÆΩ‚
|
|
ù‚∂»
|
º”ÀÆœ°·å
|
¥ŸþM(j®¨n)ÎäÎx�£¨Îx◊”ù‚∂»úp–°
|
¥ŸþM(j®¨n)ÀÆΩ‚
|
|
º”»ÎÕ¨∑NÎx◊”
|
“÷÷∆ÎäÎx
|
“÷÷∆ÀÆΩ‚
|
|
º”»ÎƒÐ∑¥ë™(y®©ng)Îx◊”
|
¥ŸþM(j®¨n)ÎäÎx
|
¥ŸþM(j®¨n)ÀÆΩ‚
|
2.≈–îýèä(qi®¢ng)»ıÎäΩ‚Ÿ|(zh®¨)µƒ∑Ω∑®“é(gu®©)¬…